Rearranjos cromossômicos, que levam à formação de um gene de fusão, foram os primeiros mecanismos de ativação de oncogenes descritos em neoplasias hematológicas em 1973, e desde então as fusões oncogênicas têm mostrado sua relevância na oncologia.
Fusões envolvendo genes como ALK, ROS1, NTRK, entre outros, são hoje importantes alvos terapêuticos em diversos tipos tumorais.
Os genes NTRK1, NTRK2 e NTRK3 codificam os três receptores da família TRK, que são denominados TRKA, TRKB e TRKC. Os receptores TRK são compostos por um domínio extracelular de ligação, uma porção transmembrana e um domínio intracelular com domínio quinase. A oligomerização dos receptores e a fosforilação de resíduos específicos de tirosina no domínio da quinase intracitoplasmática são desencadeadas quando o ligante se liga ao receptor, levando à ativação de vias de transdução de sinal, resultando em proliferação, diferenciação e sobrevivência em células neuronais normais e neoplásicas.
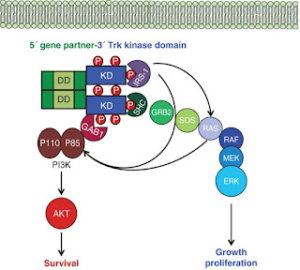
Vias de sinalização da fusão de TRK. Através das vias PI3K-AKT e MEK-ERK, as fusões de TRK conferem vantagens ao clone.
Mutações pontuais e pequenas inserções e deleções (indels) em NTRK foram descritas em vários tipos de tumores, incluindo câncer de ovário, colorretal e pulmão, bem como melanomas e leucemia mielóide. Deve-se notar, no entanto, que o papel potencial dessas mutações na promoção da tumorigênese e progressão do câncer é pouco compreendido.
Por outro lado, fusões oncogênicas envolvendo NTRK1, NTRK2 e NTRK3 foram relatadas em muitas neoplasias, de diversas histologias, e representam o principal mecanismo de ativação oncogênica de TRK. Essas fusões oncogênicas criam genes quiméricos nos quais a região 3’ do gene NTRK é unida a uma sequência 5’ de um gene parceiro de fusão e podem resultar de rearranjos intracromossômicos ou intercromossômicos.
Apesar das múltiplas possibilidades de parceiros, esses genes que se fundem a NTRK1/2/3 compartilham entre si características chave, incluindo o fato de que a quimera genética resultante mantenha o domínio NTRK quinase intacto, com os locais críticos de encaixe da tirosina preservados, e resulte em uma quinase TRK constitutivamente ativada e superexpressa. Esses genes de fusão demonstraram possuir propriedades oncogênicas, incluindo a indução da proliferação celular e a ativação de vias de sinalização relacionadas ao câncer, como as vias MAPK e PI3K/AKT/mTOR , como mostrado na figura acima.
Alterações nos genes NTRK podem induzir carcinogênese tanto em células neurogênicas quanto não neurogênicas. Essas alterações estão sendo usadas como biomarcadores preditivos para o tratamento com agentes alvo emergentes, porém, como eventos genéticos, as fusões são raramente presentes em tumores sólidos.
A prevalência da fusão do gene NTRK é inferior a 1% em tumores sólidos, mas é altamente observada em tumores raros, como carcinoma mamário secretor, carcinoma mamário secretor análogo de glândula salivar, fibrossarcoma infantil congênito (prevalência de fusão é quase 100%) e outros tumores mais raros. A fusão de NTRK está presente em aproximadamente 40% dos gliomas pediátricos não-tronco cerebrais de alto grau, mais comumente presente nos genes NTRK1 e NTRK2.
Apesar de se tratar de evento genômico raro, as respostas potenciais a inibidores de tirosina quinase são significativas. Em julho de 2019, foi aprovado no Brasil o uso do medicamento larotrectinibe (Vitrakvi®, Bayer), o primeiro inibidor seletivo de TRK para o tratamento de câncer com fusão TRK, independente da idade do paciente e do tipo tumoral. A droga está indicada para o tratamento de tumores sólidos, em pacientes adultos e pediátricos, localmente avançados ou metastáticos, que tenham fusão do gene NTRK, e é o primeiro tratamento agnóstico aprovado no Brasil.
A indicação tumor-agnóstica significa que o tumor é classificado e tratado de acordo com uma característica molecular específica e não pelo sítio-anatômico de origem ou de sua histologia.
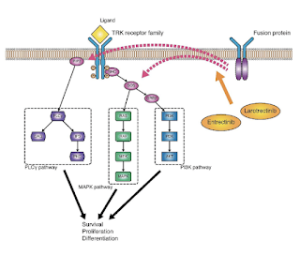
Inibidores NTRK bloqueiam a ativação das vias, mesmo com a proteína de fusão presente na célula.
A identificação de pacientes com neoplasias com fusões do gene NTRK está em constante expansão, principalmente com o advento dos inibidores de NTRK, que permitiram uma abordagem terapêutica personalizada. Sua eficácia, boa tolerância, via de administração, são fatores que levam a resultados favoráveis a longo prazo, nos diversos tipos tumorais, em cenários localmente avançadas ou metastáticos.
Ensaios com inibidores de TRK, como entrectinibe e larotrectinibe, demonstraram benefício em tumores sólidos com fusões de NTRK, com respostas parciais em 50-62% dos pacientes e respostas completas em 7-13% dos casos.
Em um estudo recente, com uma coorte de 259 casos de carcinoma de tireoide foram detectadas fusões em NTRK em 6% dos casos, e foi possível concluir que, além de guiar tratamento personalizado, a pesquisa de fusões NTRK também pode ajudar a estabelecer o diagnóstico, orientar sobre a extensão da cirurgia e sobre prognóstico.
A terapia anti-NTRK específica tem mostrado grande benefício aos pacientes, pressupondo que mesmo em se tratando de eventos raros, deva-se discutir a pesquisa de alterações em NTRK em todos os pacientes.
Veja na figura abaixo a prevalência das fusões NTRK nos diverso tipos tumorais:
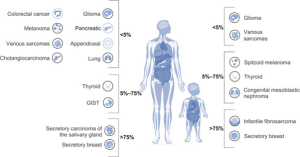
Fonte: https://doi.org/10.1016/j.jmoldx.2019.03.008
Mais uma fusão oncogênica para você não se esquecer de pesquisar no seu paciente.
Um Abraço,
Dra. Ana Carolina Paniza.
Referências bibliográficas
- Marchiò C, Scaltriti M, Ladanyi M, Iafrate AJ, Bibeau F, Dietel M, et al. ESMO recommendations on the standard methods to detect NTRK fusions in daily practice and clinical research. Ann Oncol. 2019;30(9):1417–27.
- Gatalica Z, Xiu J, Swensen J, Vranic S. Molecular characterization of cancers with NTRK gene fusions. Mod Pathol [Internet]. 2019;32(1):147–53. Available from: http://dx.doi.org/10.1038/s41379-018-0118-3
- Manea CA, Badiu DC, Ploscaru IC, Zgura A, Bacinschi X, Smarandache CG, et al. A review of NTRK fusions in cancer. Ann Med Surg. 2022 Jul 1;79.
- Bastos A, Jesus A, Cerutti J. ETV6-NTRK3 and STRN-ALK kinase fusions are recurrent events in papillary thyroid cancer of adult population. Eur J Endocrinol. 2018;178:85–93.
- Bang H, Lee M, Sung M, Choi J, An S, Kim S, et al. NTRK Fusions in 1113 Solid Tumors in a Single Institution. 2022;1–12.

